Explicamos o que é o número atômico e sua relação com a massa atômica. Além disso, o número atômico de cada elemento químico.

Qual é o número atômico?
Tanto na física quanto na química, o número atômico é o número total de prótons que compõem o núcleo atômico de um elemento químico determinado.
Geralmente é indicado pela letra Z (da palavra alemã número, “número”) e colocado como subscrito à esquerda do símbolo químico do elemento em questão, logo abaixo do número de massa A (número de núcleons no núcleo, ou seja, a soma do número de prótons e o número de nêutrons). Por exemplo:
2311Na (elemento: sódio, número atômico: 11 e número de massa: 23).
Todos os átomos são constituídos por partículas subatômicas: algumas fazem parte de seus núcleos (prótons e nêutrons) e outras giram em torno deles (elétrons). Os prótons são carregados positivamente, os nêutrons são carregados de forma neutra e os elétrons são carregados negativamente (elétrons).
Dado que os átomos na natureza são eletricamente neutroso número de partículas positivas e negativas é o mesmo, portanto, se um átomo tiver Z = 11, ele terá onze prótons e onze elétrons ao seu redor.
Além disso, o número atômico Permite organizar os elementos conhecidos na Tabela Periódica, vá do menor para o maior número de prótons no núcleo ao passar pelas linhas e colunas da tabela. Por exemplo, o hidrogênio (H) tem apenas um próton (Z = 1), enquanto o oganeson (Og) tem cento e dezoito (Z = 118). Assim, os elementos leves podem ser diferenciados dos elementos pesados.
Veja também: modelos atômicos
Exemplos de número atômico
Estes são os números atômicos da Tabela Periódica completa:
| Hidrogênio (H): Z = 1 | Hélio (Ele): Z = 2 |
| Litio (Li): Z = 3 | Berílio (Be): Z = 4 |
| Boro (B): Z = 5 | Carbono (C): Z = 6 |
| Nitrogênio (N): Z = 7 | Oxigênio (O): Z = |
| Piso (F): Z = 9 | Néon (Ne): Z = 10 |
| Sódio (Na): Z = 11 | Magnésio (Mg): Z = 12 |
| Alumínio (Al): Z = 13 | Silício (Si): Z = 14 |
| Fósforo (P): Z = 15 | Enxofre (S): Z = 16 |
| Cloro (Cl): Z = 17 | Argônio (Ar): Z = 18 |
| Potássio (K): Z = 19 | Cálcio (Ca): Z = 20 |
| Escândio (Sc): Z = 21 | Titânio (Ti): Z = |
| Vanádio (V): Z = 23 | Cromo (Cr): Z = 24 |
| Manganês (Mn): Z = 25 | Ferro (Fe): Z = 26 |
| Cobalto (Co): Z = 27 | Níquel (Ni): Z = 28 |
| Cobre (Cu): Z = 29 | Zinco (Zn): Z = 30 |
| Gálio (Ga): Z = 31 | Germânio (Ge): Z = |
| Arsénico (As): Z = 33 | Selênio (Se): Z = 34 |
| Bromo (Br): Z = 35 | Krypton (Kr): Z = 36 |
| Rubídio (Rb): Z = 37 | Estrôncio (Sr): Z = 38 |
| Itrio (Y): Z = 39 | Zircônio (Zr): Z = 40 |
| Nióbio (Ni): Z = 41 | Molibdeno (Mb): Z = 42 |
| Técnico (Tc): Z = 43 | Rutênio (Ru): Z =44 |
| Ródio (Rh): Z = 45 | Paládio (Pd): Z = 46 |
| Prata (Ag): Z = 47 | Cádmio (Cd): Z = 48 |
| Índio (In): Z = 49 | Estanho (Sn): Z = 50 |
| Antimônio (Sb): Z = 51 | Telúrio (Te): Z = 52 |
| Yodo (I): Z = 53 | Xenônio (veículo): Z = 54 |
| Césio (Cs): Z = 55 | Bario (Ba): Z = 56 |
| Lantânio (La): Z = 57 | Cério (Ce): Z = 58 |
| Praseodimio (Pr): Z = 59 | Neodímio (Nd): Z = 60 |
| Promécio (Pr): Z = 61 | Samário (Sm): Z = 62 |
| Europa (Eu): Z = 63 | Gadolínio (Gd): Z = 64 |
| Térbio (Tb): Z = 65 | Disprósio (Dy): Z = 66 |
| Holmio (Ho): Z = 67 | Erbio (Er): Z = 68 |
| Túlio (Tm): Z = 69 | Iterbio (Yb): Z = 70 |
| Lutécio (Lu): Z = 71 | Háfnio (Hf): Z = 72 |
| Tântalo (Ta): Z = 73 | Wolframio (W): Z = 74 |
| Renio (Re): Z = 75 | Ósmio (Os): Z = 76 |
| Irídio (Ir): Z = 77 | Platina (Pt): Z = 78 |
| Ouro (Au): Z = 79 | Mercúrio (Hg): Z = 80 |
| Espera (Tl): Z = 81 | Chumbo (Pb): Z = 82 |
| Bismuto (Bi): Z = 83 | Polonia (Po): Z = 84 |
| Ástato (At): Z = 85 | Radônio (Rn): Z = 86 |
| França (Fr): Z = 87 | Rádio (Ra): Z = 88 |
| Actínio (Ac): Z = 89 | Tório (Th): Z = 90 |
| Proactínio (Pa): Z = 91 | Urânio (U): Z = 92 |
| Netúnio (Np): Z = 93 | Plutônio (Pu): Z = 94 |
| Américo (Am): Z = 95 | Curiosidade (Cm): Z = 96 |
| Berkelio (Bk): Z = 97 | Califórnia (Cf): Z = 98 |
| Einsteinium (Es): Z = 99 | Férmio (Fm): Z = 100 |
| Mendelevio (Md): Z = 101 | Nobel (Não): Z = 102 |
| Laurencio (Lr): Z = 103 | Rutherfordio (Rf): Z = 104 |
| Dúbio (Db): Z = 105 | Seaborgio (Sg): Z = 106 |
| Bohrio (Bh): Z = 107 | Hassing (Hs): Z = 108 |
| Meio Ambiente (Mt): Z=109 | Darmstatio (Ds): Z = 110 |
| Roentgênio (Rg): Z = 111 | Copérnico (Cn): Z = 112 |
| Nihomio (Nh): Z = 113 | Fleróvio (Fl): Z = 114 |
| Moscou (Mc): Z = 115 | Livermorio (Lv): Z = 116 |
| Tennessee (Ts): Z = 117 | Oganeson (Og): Z = 118 |
número de massa e massa atômica
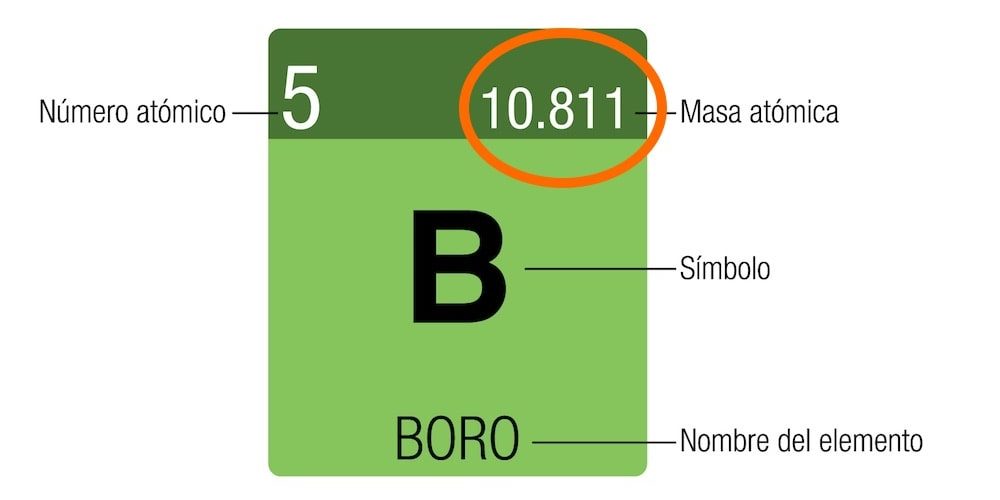
O número de massa é a soma de prótons e nêutrons.. É indicado pela letra A (do alemão Atomgewicht) como sobrescrito à esquerda do símbolo químico (por exemplo: 23já).
Número de massa é geralmente cerca de duas vezes o número atômico uma vez que os nêutrons fornecem estabilidade ao núcleo atômico e, assim, superam a repulsão natural entre prótons carregados positivamente. Ao contrário do número atômico, o número de massa varia em cada isótopo.
O número de massa pode ser calculado de acordo com a fórmula:
Número de massa (A) = número atômico (Z) + número de nêutrons (N).
O número de massa não deve ser confundido com a massa atômica. A massa atômica é medida em unidades amu. (unidade de massa atômica) o Da (Dalton). Esta unidade é calculada a partir do átomo de carbono e cada amu é um doze avos de sua massa. A tabela periódica lista a massa atômica do isótopo mais estável.
Continuar com: Valência em química
Referências
- “Número atômico” na Wikipedia.
- “Número atômico, número de massa e isótopos” na Khan Academy.
- “Qual é o número atômico?” em Clickmica, perguntas e respostas sobre química.
- “Understanding Atomic Number and Atomic Mass” (vídeo) na Ricochet Science.
- “Número atômico” na Enciclopédia Britânica.
